
 |
|
Читаемые статьи
Читаемые книги
Ссылки
|
Главная > Процесс соединения металлических деталей углерода и особенно марганца в присадочной проволоке или покрытии электрода значительно снижает содержание азота в наплавленном металле. При сварке электродами с качественными покрытиями содержание азота в металле незначительно и составляет всего 0,005- 0,015%. Сера является вредной примесью в стали. Она образует сернистое железо (сульфид железа FeS), которое имеет температуру плавления 1193°, т. е. более низкую, чем сталь. Поэтому при кристаллизации стали сернистое железо остается еще в жидком вцде в прослойках между кристаллами сплава и является одной из причин образования горячих трещин при сварке. Серу удаляют введением марганца, который образует с ней химическое соединение - сернистый у марганец (MnS) по реакциям: FeS-l-Mn;f*MnS + Fe; FeS -{- МпО 5 MnS + FeO. Сернистый марганец не растворяется в жидком металле и полностью переходит в шлак. Удалению серы способствует также окись кальция, при этом происходит реакция FeS4-CaO = FeO-i-CaS. Присутствие фосфора вызывает неоднородность металла шва, рост зерен и снижение пластичности, особенно при низких температурах (хладноломкость). Он присутствует в металле шва в виде фосфидов железа: FcgP и FcgP. Удаление фосфора происходит при реакциях: с закисью железа . . 2 FeP -\- 5 FeO = PgOj 9 Fe или........2 FcgP + 5 FeO = PO +llFe; с окисью кальция . . 3 СаО -\- PgOj = CagPgOg или........4 СаО + PgOg = Са4Р20в Получаемые соединения фосфора переходят в шлак. Основные шлаки лучше удаляют фосфор из металла, чем кислые. Водород является вредной примесью в стали. При температуре дуги водород диссоциирует на атомы и, находясь в атомарном состоянии, способен хорошо растворяться в наплавленном металле. При остывании и затвердевании металла атомы водорода вновь соединяются в молекулы, которые собираются в отдельных местах шва, образуя газовые пузырьки. Водород не всегда успевает полностью выделиться из металла и вызывает появление в нем пористости и мелких трещин, так называемых флокенов. Сталь с флокенами является хрупкой, в изломе флокены имеют вид светлых пятен и не выявляются обычно применяемыми методами контроля качества швов без разрушения. По мере увеличения температуры металла растворимость водо- рода увеличивается, достигая наибольшей степени при 2400°. Насыщение металла водородом происходит в основном в момент переноса капель металла в дуге. В 100 г металла может раствориться до 43 с} водорода. При содержании водорода до 6,5 на 100 г металла шов получается плотным; при более высоком насыщении металла водородом появляются пористость, флокены, снижается пластичность, металл становится хрупким в холодном состоянии. Источником насыщения металла водородом является влага, содержащаяся в электродном покрытии, флюсах и окружающем воздухе или находящаяся на поверхности свариваемого металла в виде воды, снега, инея. Кроме того, вЬдород содержится в ржавчине, которая может быть на сварочной проволоке или кромках металла. Наимене-е металл насыщается водородом при сварке на постоянном токе обратной полярности, наиболее - при сварке на переменном токе. Это обусловлено тем, что при сварке на переменном токе в момент перехода тока через нулевое значение жидкий металл не защищен действием электрического поля дуги и доступен для растворения в нем атомов водорода, несущих отрицательный заряд электричества. Чтобы предотвратить насыщение металла водородом при сварке стали необходимо следующее: 1. Обеспечить минимальное содержание влаги в покрытии и флюсах, в окружающей шов атмосфере и на кромках металла. С этой целью применяемые для сварки электроды следует тщательно просушивать путем прокалки. Для покрытий основного типа (УОНИ и др. см. § 2 гл. VI) прокалку ведут при 350° в течение 5 час. Хранить электроды следует в сухом месте, а при их увлажнении вновь подвергать прокалке перед выдачей сварщику. Желательно, чтобы сварщики при работе на открытом воздухе имели герметически закрывающиеся футляры для хранения электродов. При работе под дождем и снегом места сварки должны быть надежно защищены ст попадания влаги палатками из брезента, фанеры и других материалов. Перед сваркой необходимо тщательно протирать и просушивать кромки металла, не оставляя на,них влаги. При сварке труб концы их нужно закрывать деревянными пробками, чтобы не допустить циркуляции влажного воздуха внутри трубы и подсоса его из трубы в шов. 2. Использовать проволоку без ржавчины и удалять ее с кромок свариваемого металла. 3. Стараться не применять многопроходных швов при автоматической сварке под флюсом, так как при наложении последующих слоев водород насыщает нижележащие слои в момент их расплавления. Атомарный водород может также раскислять металл, например, по реакции FeO-f 2H = Fe-f НО. 3. Строение сварного шва Наиболее широкое применение в сварных конструкциях имеет малоуглеродистая сталь. Рассмотрим поэтому вопрос о строении сварного шва на примере сварки малоуглеродистой стали. Основой стали является железо, в котором размещены частицы углерода и других элементов, входящих в ее состав. Железо может находиться в стали в виде феррита и аустенита. Ферритом называется чистое железо, очень мягкое, обладающее высокой пластичностью, прочностью и магнитными свойствами. В виде феррита железо может находиться при температуре до 910°. Атомы кристалла феррита расположены по схеме, показанной на рис. 25, а. При температуре 910° (назывемой критической) и выше феррит переходит,в аустенит, характеризуемый более уплотненньм расположением атомов (рис. 25, б). Аустенит не магнитен и отличается большей твердостью и вязкостью. При охлаждении ниже 910 аустенит способен снова превращаться в феррит. Углерод содержится в стали в виде химического соединения с железом - цементита (FegC), отличающегося высокой твердостью и хрупкостью. Цементит в мягкой малоуглеродистой стали располагается в виде очень тонких пластинок, скопления которых распредачены в основной массе феррита. Такое строение (структура) стали называется перлитом, представляющим собой механическую смесь феррита с цементитом. По мере увеличения содержания углерода в стали количество перлита в ней возрастает. Сталь, содержащая 0,83% углерода, состоит только из перлита. При дальнейшем повышении содержания углерода начинается выделение отдельных зерен цементита и структура стали будет состоять из перлита с распределенным в нем цементитом. Углерод понижает критическую температуру. Как указывалось вьшхе, для чистого железа она равна 910°, для стали, содержащей 0,9% углерода, она составляет всего 720°. Аустенит способен хорошо растворять углерод, вследствие чего при нагревании стали до температуры, незначительно (на 20-30°) превышающей критическую, включения цементита исчезают и сталь приобретает равномерную мелкозернистую структуру. Если затем сталь медленно охладить, то она сохранит мелкозернистое строение. Это свойство 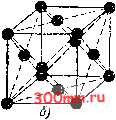 Рис. 25. Схема расположения атомов в кристалле железа: о - феррита, б - аустенита
|
 Чем хороши многотопливные котлы?  Нетрадиционное отопление  Детище отечественной Оборонки  Что такое автономное индивидуальное отопление?  Использование тепловых насосов  Эффективное теплоснабжение для больших помещений  Когда удобно применять теплые полы |
|
© 1998 - 2026 www.300mm.ru.
При копировании материала обязательно наличие обратных ссылок. |